宫腔粘连(IUA),又称Asherman综合征,是育龄女性常见的子宫内膜损伤性疾病,常导致月经异常、不孕或反复流产,严重影响女性的生殖健康与生活质量。传统治疗手段如宫腔镜下粘连分离术虽能恢复宫腔形态,但术后高复发率及内膜修复不良仍是临床面临的严峻挑战。随着再生医学的蓬勃发展,以干细胞为基础的治疗策略为IUA的根治带来了革命性希望,正从基础医学研究快速走向临床试验与发展阶段。
一、 干细胞疗法的理论基础与核心机制
干细胞治疗宫腔粘连的核心逻辑在于利用其强大的自我更新、多向分化潜能以及旁分泌功能。主要应用的干细胞类型包括:
- 骨髓间充质干细胞(BM-MSCs):研究历史最长,证据较为丰富。可通过静脉灌注或宫腔局部移植,归巢至损伤部位,分化为子宫内膜上皮细胞和基质细胞,并通过分泌血管内皮生长因子(VEGF)、肝细胞生长因子(HGF)等因子,促进血管新生、抑制纤维化、调节局部免疫微环境,从而修复受损内膜,改善容受性。
- 脂肪来源间充质干细胞(AD-MSCs):具有取材方便、来源丰富、增殖能力强等优点。其修复作用同样依赖于分化替代与旁分泌效应,在动物模型中已证实能有效减少纤维化面积,增加内膜厚度与腺体数量。
- 经血来源子宫内膜干细胞(MenSCs):源自女性经血,具有子宫内膜源性、无创获取、免疫原性低等独特优势。因其与子宫内膜组织同源,在定向分化为内膜细胞方面可能更具潜力,是当前研究的热点。
- 脐带间充质干细胞(UC-MSCs):具有更强的增殖能力和更低的免疫原性。其分泌的胞外囊泡(外泌体)作为无细胞治疗剂,携带多种生物活性物质,能够模拟干细胞的治疗作用,避免了细胞移植的潜在风险,成为新兴研究方向。
二、 临床前研究与动物模型验证
大量临床前研究在小鼠、大鼠、兔等动物IUA模型中验证了各类干细胞的安全性与有效性。研究普遍显示,干细胞移植后,实验动物的子宫内膜厚度、腺体密度、血管化程度显著改善,纤维化标志物(如胶原蛋白)表达下降,妊娠结局得到提升。这些研究不仅阐明了作用机制,也为临床试验剂量、途径(如宫腔灌注、支架材料复合移植等)的选择提供了关键依据。
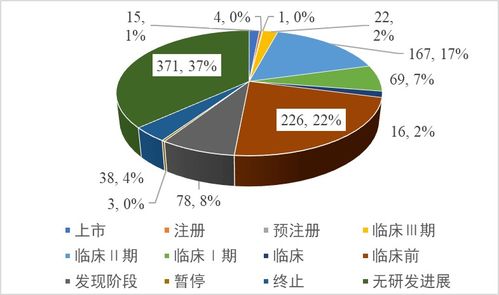
三、 临床试验的现状与初步成果
干细胞治疗IUA已步入临床研究阶段。全球范围内已注册多项早期临床试验(I/II期),主要在中国、伊朗、埃及等国家开展。这些试验初步证明了自体或异体MSCs(尤其是BM-MSCs和UC-MSCs)宫腔移植的安全性、可行性和潜在疗效。
当前临床转化模式主要包括:
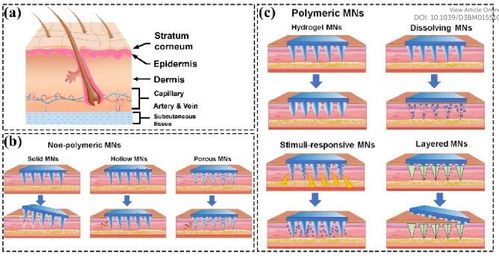
- 单纯干细胞悬液宫腔灌注:操作相对简便。
- 复合生物支架材料移植:将干细胞负载于胶原支架、羊膜、水凝胶等可降解材料上,构建组织工程化内膜,旨在为细胞提供更佳的生长微环境并实现物理屏障作用,防止再粘连,是目前最具前景的策略。
已报道的初步临床效果:多数研究显示,接受干细胞治疗的患者宫腔形态得到更好维持,内膜血流与厚度增加,部分长期不孕患者成功实现了自然妊娠或通过辅助生殖技术分娩健康婴儿。现有试验样本量普遍较小,缺乏长期随访和大规模、多中心、随机双盲的III期临床试验数据,疗效的稳定性和普适性仍需进一步证实。
四、 面临的挑战与未来发展方向
尽管前景广阔,干细胞疗法全面应用于IUA临床仍面临诸多挑战:
- 治疗标准化问题:干细胞的最优来源、最佳剂量、最佳移植时机(月经周期阶段)、最佳递送方式(细胞悬液 vs. 组织工程复合物)尚未统一。
- 长期安全性与机制深化:需明确移植细胞的体内长期命运、潜在的致瘤风险、免疫排斥反应(尤其在异体移植中)以及表观遗传学影响。治疗的确切分子机制,特别是旁分泌作用的具体信号通路网络,有待更精细的解析。
- 监管与伦理:作为先进的细胞治疗产品,其制备、质检、临床应用的规范需严格遵守国家药品监管机构(如中国NMPA、美国FDA)的指南,确保生产流程的标准化与质量可控。
- 成本与可及性:治疗成本较高,限制了其普及。开发“现货型”的异体干细胞产品或更经济高效的无细胞疗法(如外泌体)是重要方向。
五、 结论与展望
干细胞疗法为宫腔粘连这一难治性疾病开辟了极具潜力的再生治疗新路径。从基础研究到临床试验,证据链正在不断完善。该领域的研究将更加聚焦于:优化细胞来源与制备工艺;开发智能型生物活性支架材料;深入探索无细胞治疗策略;以及通过严谨的大规模临床试验确立金标准治疗方案。随着再生医学、材料科学与临床医学的深度融合,干细胞疗法有望在未来十年内成为宫腔粘连标准化治疗的重要组成部分,从根本上修复“生命土壤”,守护女性生殖健康。